SMILES™ i Jmol: els estàndards per a la representació de molècules orgàniques a Internet
SMILES™ i Jmol a Internet
Podem trobar molts exemples de l'ús d'SMILES™ i Jmol a Internet
ChemSpider
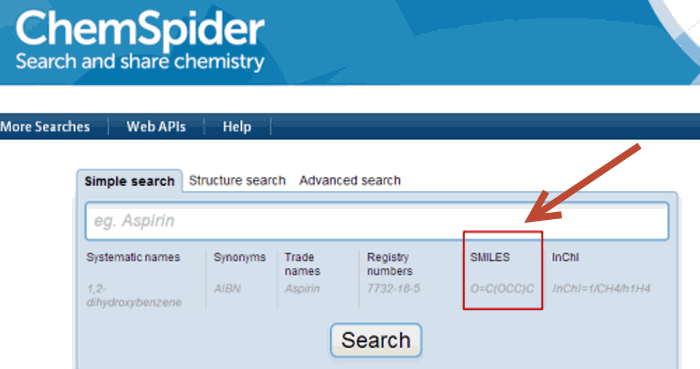
PubChem
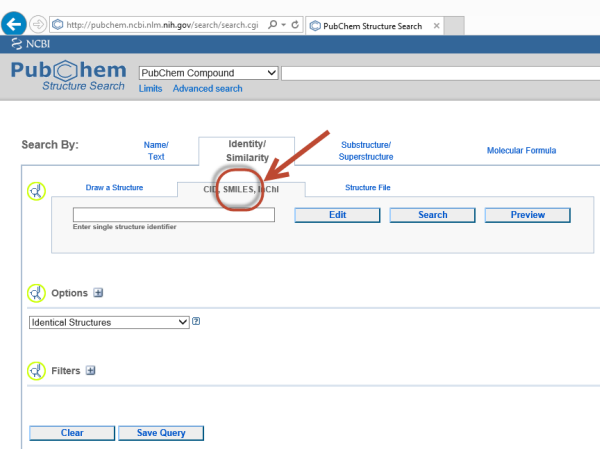
eMolecules
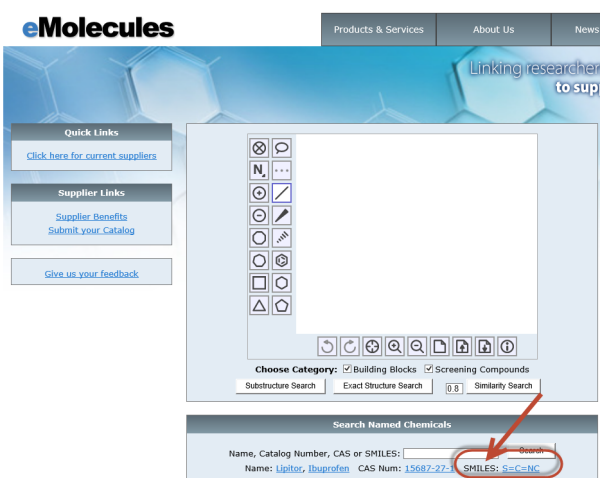
Wikipedia
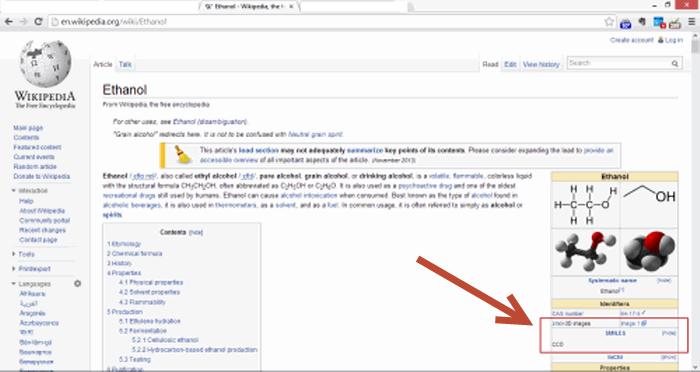
Petit Tutorial d'SMILES™

SMILES™ va ser creat per David Weininger, al Laboratori de Recerca Ambiental, U.S.E.P.A., Duluth, MN a finals dels anys vuitanta; el disseny es va completar al Pomona College, Claremont, CA. Es va incorporar al Daylight Toolkit amb l'assistència de Cedar River Software.
SMILES™ vol dir, en anglès, Simplified Molecular Input Line Entry System (sistema simplificat d'entrada en línia de molècules)
SMILES™ és un llenguatge químic molt senzill, en el qual les molècules i reaccions poden ser especificades fent ús de caràcters ASCII que representen enllaços i àtoms.
SMILES™ conté la mateixa informació que d'altres llenguatges, però amb alguns avantatges. Una línia de SMILES™ és molt fàcilment comprensible, molt compacta, i amb la possibilitat d'intuir un patró que representi un identificador universal per a una estructura química específica.
Els paréntesis són utilitzats per a indicar punts de bifurcació i etiquetes numèriques les quals designen localitzacions específiques de funcions. La gramática bàsica de SMILES™ també inclou informació isotòpica, la configuració de dobles enllaços i la quiralitat que ens porta al món dels estereoisòmers.
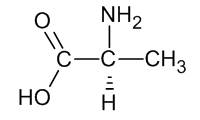
Alguns exemples molt senzills de SMILES™ són:
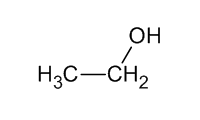 |
|||
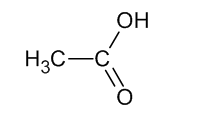 |
|||
 |
|||
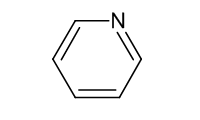 |
|||
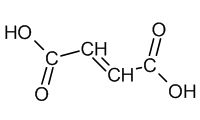 |
|||
 |
Des de que coneixem aquest llenguatge, SMILES™ ha experimentat algunes modificacions i ampliacions per tal d'incloure no només noves possibilitats sinó dos llenguatges químics adicionals: SMARTS®, una ampliació de SMILES™ que permet especificacions a les subestructures moleculars, i SMIRKS®, una versió restringida de SMARTS® què inclou canvis en els enllaços atòmics de reaccions genèriques.
NORMES D'ESCRIPTURA
La notació de SMILES™ consisteix en una sèrie de caràcters que no contenen espais entre ells. Els àtoms d'hidrogen poden ser omesos.
Es poden establir 5 categories diferents: àtoms, enllaços, radicals, estructures cícliques i compostos iònics. Les normes per especificar les isomeries les comentarem més endavant.
Àtoms:
Els àtoms es representen amb els seus símbols atòmics.
Cada element s'ha d'especificar amb el seu símbol atòmic (la segona lletra, si cal, ha de ser una minúscula) entre claudators, [ ], amb l'exepció de l'hidrogen.
Els elements més habituals a la Química Orgànica: B, C, N, O, P, S, F, Cl, Br i I es poden escriure sense claudators quan es treballa amb la valència més petita d'aquests elements: B (3), C (4), N (3,5), O (2), P (3,5), S (2,4,6) i 1 pels halògens.
Els àtoms que pertanyen a anells aromàtics s'escriuen amb minúscules.
Com que en absència de claudators hem de suposar els hidrogens necessaris, es consideren vàlides les següents notacions:
Els àtoms que actuen amb valències diferents a les anteriorment indicades, i els elements que habitualment no formen part de la Química Orgànica han de ser escrits obligatòriament fent servir els claudators.
Qualsevol hidrogen enllaçat i també les càrregues formals s'han d'indicar sempre fent servir claudators. El nombre d'hidrogens es mostra amb el símbol H seguit per un dígit (és opcional). De manera similar, una càrrega formal es mostra amb els símbols + o -, seguits per un dígit (opcional). En cas de no especificar el nombre d'hidrogens i la càrrega, es considerarà zero per a qualsevol àtom dins d'uns claudators.
Es consideren iguals les construccions [Fe+++] i [Fe+3].
Alguns exemples són:
Enllaços:
Els enllaços senzills, dobles i triples es representen pels símbols: -, = i #, respectivament.
Els àtoms adjacents es suposen connectats entre sí per un enllaç senzill i normalment no s'especifica.
Alguns exemples són:
A l'hora d'escriure estructures lineals, la notació SMILES™ permet fer omissió dels hidrogens i dels enllaços senzills. Per exemple, 6-hidroxi-1,4-hexadiè pot ser representat per molts SMILES™ igualment vàlids, inclosos els tres següents:
| C=CCC=CCO | |
| OCC=CCC=C |
Radicals:
Els radicals o ramificacions s'especifiquen entre paréntesi, i poden ser anidats o apilats. En qualsevol cas, un radical escrit entre paréntesi sempre s'ha de considerar connectat a l'àtom de l'esquerra.
Alguns exemples són:
 |
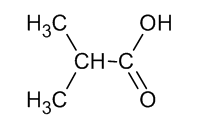 |
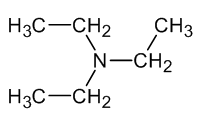
| CCN(CC)CC | CC(C)C(=O)O |
| Trietilamina | Àcid isobutanoic |
Estructures cícliques:
Les estructures cícliques alifàtiques es representen mitjançant la ruptura d'un enllaç en cada anell. Els enllaços estan numerats en qualsevol ordre, indicant els enllaços del principi i del final de l'anell mitjançant un dígit a continuació del símbol de l'àtom. El ciclohexà és un típic exemple (C1CCCCC1):
Respecte dels anells aromàtics, l'alternança d'enllaços senzills i dobles s'indica escrivint els àtoms de l'anell en minúscules. D'aquesta manera, el benzè quedaria així: (c1ccccc1)
De vegades hi ha diverses maneres d'escriure en SMILES™ una mateixa estructura, variant el "tancament" de l'anell en diferents àtoms. SMILES™ no té entrades preferencials, però s'intenta representar les estructures de manera senzilla.
Ens podem trobar certes estructures amb més d'un àtom de "tancament", com per exemple l'estructura d'una molècula com ara el cubà (C12C3C4C1C5C4C3C25):
 ALC-CGE 2013
ALC-CGE 2013